
APPLICATIONS DES NANOTECHNOLOGIES À LA MÉDECINE
Le recours à des nano objets concernerait déjà près de 10 % du volume des marchés médicaments, diagnostics et instrumentations médicaux confondus. Toutefois, la part de médicaments est – n’en déplaise à des gourous influents de la Silicon Valley – très en-deçà de l’imaginaire du grand public. La recherche est portée par l’espoir de surmonter quelques limitations des approches « traditionnelles », moyennant parfois des « tickets d’entrée » modérés.
L'approche « classique » de la médecine rencontre des limitations qui tendent à dégrader le ratio effets secondaires / efficacité, à inhiber des effets attendus et à générer des résistances. Ces limitations proviennent de la dégradation par l’organisme (métabolisation), d’où une faible disponibilité ; d’un ciblage large, d’où une faible spécificité ; voire de limitations à l’accès aux zones concernées par les mécanismes biologiques clé. Ces limitations proviennent notamment de la métabolisation des produits par l’organisme, qui réduit leur disponibilité, d’un ciblage insuffisamment spécifique et de difficultés d’accès aux zones concernées.
En permettant de mieux maîtriser l’intégration par l’organisme d’objets de taille comparable à celle des zones « cibles » visées (entre 1 et 100 nm), les nanotechnologies permettent d’aller au plus près des mécanismes biologiques, de réduire dans des proportions drastique le dosage, les effets secondaires et les résistances – voire même de les contourner lorsqu’elles se manifestent – . Elles ouvrent aussi des horizons très riches en médecine personnalisée. Les champs les plus actifs de la R&D à ce jour sont les suivants :
- dépistage et traitement de cancers (bio-marqueurs, imagerie, contournement des résistances, réduction des effets secondaires, etc.) ;
- instrumentation, qui porte un très fort potentiel de productivité de R&D pharmaceutique (criblage, tests) et d’applications pour comprendre les mécanismes de dégénerescence en neurologie ;
- médecine régénérative et biomatériaux (prothèses et tissus implantables « fonctionnalisés ») ;
- traitement de maladies cardiovasculaires et du diabète (amélioration des procédés de délivrance au plus près des zones à activer, minimisation des effets secondaires et des contraintes pour l’utilisateur, etc.) ;
- donner une deuxième vie à des antibiotiques devenus inopérants suite à l’apparition de résistances.
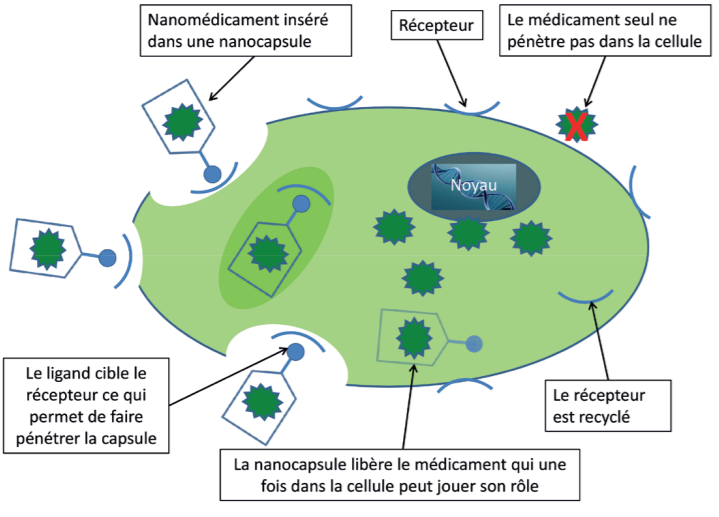
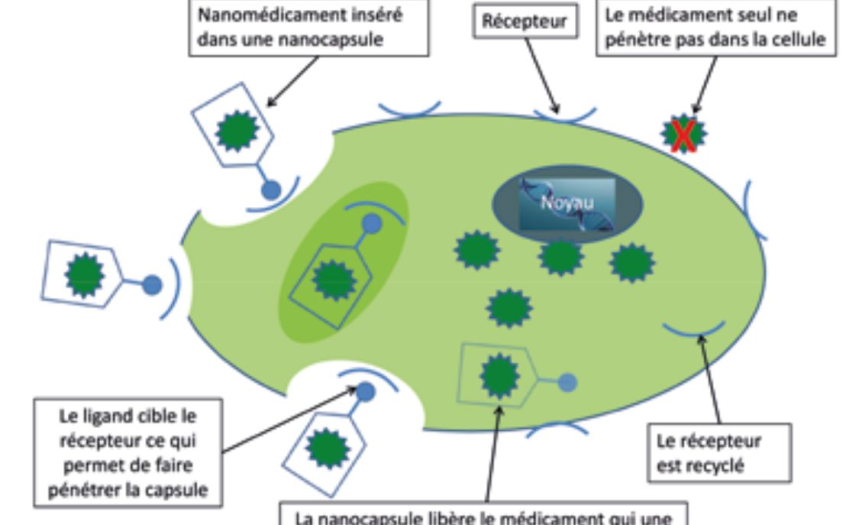
Exemple de fonctionnement d’un nano médicament
Il est donc surtout question de diagnostics et d’instrumentation
On notera, en effet, que tout médicament candidat à la commercialisation doit passer le filtre touffu de l’autorisation de mise sur le marché (AMM), ce qui se traduit par un « ticket d’entrée » en général très supérieur au milliard d’euros. En ces termes, un projet de nano médicament ne sera pas vraiment mieux loti car, même si le processus pourrait être mieux sécurisé, voire accéléré du fait d’une meilleure spécificité, il faudra quand même prévoir une bonne décennie entre le concept et la commercialisation, sans compter d’éventuels tests complémentaires pour prouver la totale innocuité des nano éléments utilisés.
La réglementation pénalise moins le processus d’innovation en diagnostics et instrumentation, dont le déroulement, du concept jusqu’à la mise sur le marché, représente un investissement de l’ordre de 10 à 100 M€. Toutefois, ce processus pourra être compliqué par l’existence de brevets préexistants, auquel cas il faudra prévoir des coopérations en amont.
Le paysage des acteurs européens est riche, mais très fragmenté
L’Europe compte 2 000 acteurs, dont 800 centres de R&D et autant d’entreprises (France et Allemagne 350 chacune, Royaume Uni 150, Italie 100)… contre 120 acteurs en Amérique du nord !
Au-delà de ces chiffres, d’importantes disparités de taille et surtout d’environnement existent (notamment financement de l’innovation). On notera que la première « pharma » européenne, Roche, dont la filiale Diagnostics est leader mondial en micro et nano-instrumentation, se détache nettement d’une myriade d’acteurs en émergence. Cela laisse espérer que Roche sera très apte à exploiter les complémentarités entre nano-fluidique et pharmacie.
En France, deux pôles forts se détachent : Île de France (60 acteurs) et axe Lyon-Grenoble (60 acteurs, la moitié autour du pôle Minatec). Aux Etats-Unis, les leaders des NBICs sont très impliqués en nano médecine. Toutefois, les nanotechnologies font un peu figure d’exception qui confirme la règle selon laquelle la détention d’une capacité informatique considérable (information ou capacité à la traiter) conférerait à leurs titulaires une capacité à pérenniser leur leadership sur les plate-formes des marchés futurs. Un espace de collaboration sincère existe donc avec les leaders des NBICs !
| LA TOXICITÉ DES NANO PARTICULES : UNE QUESTION ENCORE MAL ÉLUCIDÉE |
|
Les atteintes possibles de nano particules aux cellules sont relativement bien identifiées in vitro, notamment : réactions oxydatives, atteinte au matériel génétique, dénaturation des mécanismes d’échanges aux interfaces. Mais les risques effectifs posés à l’organisme et à l’environnement sont entachés d’incertitudes très fortes. Sont en cause, le réalisme des expériences in vitro (conditions et concentrations en jeu), la complexité des phénomènes d’accumulation et d’agrégation dans l’organisme et l’environnement, les difficultés à discriminer les différents mécanismes mis en jeu et à appréhender les effets de temps long. Les preuves de risque ou d’innocuité des nano particules sont donc rares. L’amiante et les suies des cheminées et des moteurs à explosion font figure d’exceptions notables. Dominique LUZEAUX, IGA et Frédéric TATOUT, ICA |
En nano médecine, l’Europe semble donc garder quelques chances de ne pas se faire vassaliser par des acteurs US, même s’il est urgent de promouvoir la structuration d’un écosystème en Europe. Qu’en est-il ?
L’Europe a publié une une roadmap et instauré une plate-forme technologique basée à Paris Vème, efficace pour accélérer le processus d’innovation (www.etp-nanomedicine.eu), ce qui semble adapté à la structure des acteurs, même si on note l’absence d’une 1 Les nanotechnologies bénéficient relativement peu, à ce jour, des effets de réseau, qui démultiplie le leadership industriel. De plus, la barrière financière à l’entrée reste relativement modique en-dehors du domaine des médicaments. thématique dédiée dans le cadre d’Horizon 2020.
En France, l’action des pouvoirs publics semble à la hauteur des enjeux, avec le pôle Minatec, mais les acteurs pourraient accentuer leur présence sur les débouchés en instrumentation, secteur qui a le sentiment d’avoir été « abandonné » de longue date, dans lequel quelques centres de recherche d’excellent niveau subsistent – jusqu’à quand ?
Il est aussi souhaitable qu’une réflexion éthique se développe, même si les risques de dérapage médiatique semblent faibles à ce jour. C’est heureusement le cas, du moins, en Europe. Surtout, vu le décalage entre mythe et réalité, tous les acteurs doivent soigner la communication afin de ne pas effrayer les citoyens et ne pas décevoir les attentes des marchés. Car nous n’en sommes qu’au tout début…
 |
Frédéric TATOUT, ICA |
| Après un début de carrière scientifique et technique au CEA et à la DGA, Frédéric Tatout a été responsable du développement d’usages numériques au ministère de l’industrie. Retourné à la DGA comme responsable de secteur industriel il dirige des projets innovants pour améliorer la performance du MCO aéronautique au sein du ministère de la défense. | |






















Aucun commentaire
Vous devez être connecté pour laisser un commentaire. Connectez-vous.